L’immense force de cette étude réside dans son modèle expérimental : là où la majorité des études antérieures se limitaient à simuler des DOMS légers par contractions volontaires, ici les chercheurs ont reproduit une véritable lésion musculaire avec nécrose myofibrillaire, validée histologiquement.
Pour cela, 34 participants sains, anciens sportifs désentraînés, ont été soumis à un protocole d’excentrique électriquement stimulée ciblant le quadriceps, créant des lésions fibreuses authentiques comparables aux lésions cliniques musculaires rencontrées dans le sport
.
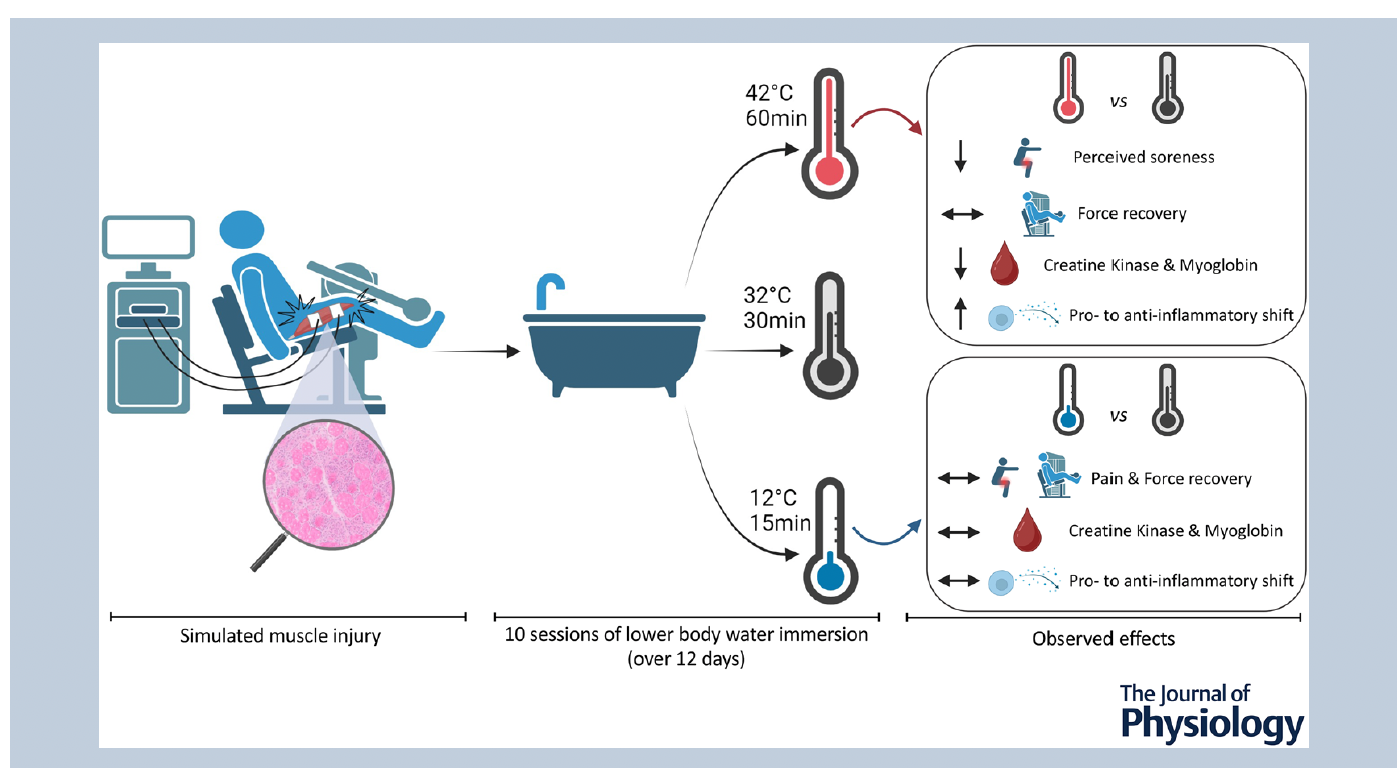
Les sujets ont ensuite été répartis en trois groupes de traitement post-lésion :
- Bain froid (CWI) : 12°C pendant 15 minutes.
- Bain thermoneutre (TWI) : 32°C pendant 30 minutes.
- Bain chaud (HWI) : 42°C pendant 60 minutes.
Chaque protocole a été appliqué pendant 12 jours consécutifs avec un suivi extrêmement complet : biopsies musculaires (avant, J5, J11), scores de douleur, force musculaire et analyses moléculaires sanguines et histologiques.
La force musculaire
La récupération mécanique brute n’a été accélérée par aucun des traitements. À 10 jours, la force maximale restait diminuée d’environ 32% dans les trois groupes
.Ce résultat rappelle qu’en phase aiguë, la force n’est pas un indicateur sensible de la qualité biologique de la régénération.
La douleur
Le groupe bain chaud (HWI) est le seul à avoir montré une réduction significative de la douleur perçue à la palpation et aux mouvements fonctionnels. Aucun effet analgésique n’a été retrouvé avec le bain froid.
Les biomarqueurs sanguins de lésion musculaire
- Les taux de créatine kinase (CK) et de myoglobine étaient significativement plus bas sous bain chaud dès J4 et J8, montrant une réduction de l’extension des lésions secondaires.
- Le froid n’a eu strictement aucun effet sur ces marqueurs.
La régulation de l’inflammation
- Le bain chaud a permis une élévation significative de l’IL-10, cytokine clé de la phase de résolution anti-inflammatoire.
- Le bain froid maintenait une activation plus prolongée du facteur NF-κB p65, favorisant la persistance d’une inflammation non résolue.
Les protéines de choc thermique (HSP)
L’immersion chaude a induit une sur-expression des HSP27 et HSP70, protéines de protection cellulaire favorisant la stabilisation du cytosquelette musculaire lésé, la limitation des dommages secondaires et l’optimisation de la réparation tissulaire.
Aucun effet délétère sur la fibrose
Aucun groupe n’a présenté d’élévation anormale de TGF-β1, marqueur de fibrose musculaire, confirmant la sécurité du bain chaud en termes de cicatrisation tissulaire
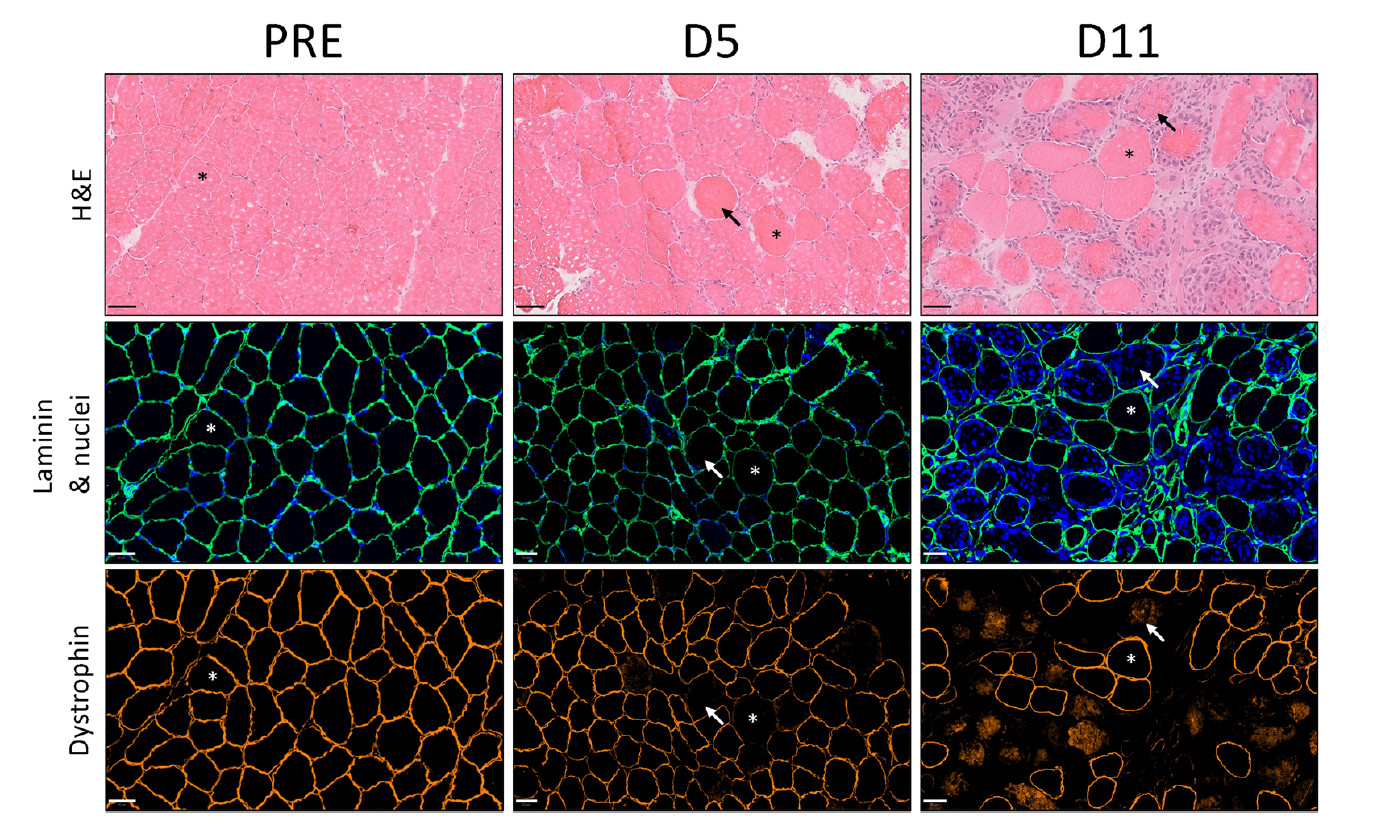
La Figure 2 illustre l'évolution du muscle lésé avant et après la lésion expérimentale. Avant la lésion (PRE), le tissu musculaire apparaît homogène et bien structuré, avec des fibres musculaires polygonales régulières et des noyaux localisés en périphérie. À cinq jours (D5), les premières altérations sont nettes : certaines fibres gonflent, perdent leur forme polygonale normale et montrent des noyaux qui migrent vers l’intérieur de la fibre. La membrane musculaire, marquée ici par la dystrophine et la laminine, présente déjà des zones de rupture et de désorganisation.
À onze jours (D11), les lésions initiales persistent encore sur une partie des fibres, mais on observe clairement les signes d'une réparation en cours. Les noyaux restent souvent centrés — marqueur classique de la régénération musculaire — tandis que la membrane périphérique commence à se réorganiser. Toutefois, certaines fibres restent partiellement nécrotiques ou montrent encore une perte de dystrophine membranaire. Cette cinétique histologique confirme que le protocole utilisé induit une vraie lésion musculaire nécrosante et permet d’évaluer finement l’impact des différentes modalités de récupération appliquées dans l’étude.
Longtemps associé à tort à une récupération accélérée, le froid présente plusieurs limitations physiologiques dans ce contexte précis :
- Réduction du flux sanguin local.
- Inhibition de certaines voies cellulaires adaptatives.
- Ralentissement de la transition inflammatoire vers la reconstruction.
- Absence de stimulation des protéines de choc thermique nécessaires.
Le froid reste utile en phase de gestion aiguë hémorragique ou sur certaines contusions, mais montre ici une absence d’effet sur la régénération myofibrillaire.
Les bénéfices physiologiques de l’immersion chaude reposent sur plusieurs mécanismes synergiques :
- Vasodilatation et meilleure perfusion musculaire locale.
- Accélération de la clairance métabolique des débris cellulaires.
- Activation des HSP, véritables protecteurs cellulaires.
- Modulation favorable de la cascade inflammatoire et transition rapide vers la phase de réparation tissulaire.
- Maintien de l’intégrité structurale et préservation fonctionnelle des fibres musculaires.
En résumé, la chaleur ne se contente pas de soulager, elle agit directement sur la biologie de la réparation musculaire.
L’équipe scientifique de Kinesport a réalisé une relecture critique approfondie de cette étude.
L’ensemble du protocole expérimental est globalement très bien conduit :
- Le modèle de lésion musculaire est pertinent et reproduit fidèlement une atteinte clinique observable.
- Les mesures biologiques, histologiques et fonctionnelles sont extrêmement détaillées et robustes.
- La randomisation exacte des participants n’est pas entièrement détaillée par les auteurs, mais les groupes étaient parfaitement homogènes à l’inclusion, réduisant significativement tout biais d’allocation.
- Aucun conflit d’intérêt ou biais majeur détecté.
➡ L’étude bénéficie d’une validité scientifique et peut être considérée comme importante dans la réflexion thérapeutique autour des lésions musculaires nécrosantes.
Les données permettent désormais de faire évoluer nos pratiques terrain :
- Intégrer le bain chaud (42°C pendant 60 minutes) dans les 10 à 14 jours suivant une déchirure musculaire.
- Limiter l’usage du froid aux seules phases initiales hémorragiques ou d’œdème.
- Associer la stratégie thermique à une mise en charge progressive adaptée et à une réathlétisation fonctionnelle raisonnée.
- Moduler finement la charge inflammatoire selon le stade de réparation.
La chaleur régule activement la biologie de la régénération musculaire.Le bain chaud stimule les protéines HSP, module favorablement l’inflammation (IL-10 ↑, NF-κB ↓) et optimise l’environnement cellulaire de réparation.
Le bain froid n’apporte aucun bénéfice régénératif sur les lésions musculaires nécrosantes.
Aucune amélioration de la force, de la douleur, ni des biomarqueurs de dommage musculaire sous cryothérapie.
Les protocoles classiques RICE/POLICE manquent toujours de validation scientifique sur la régénération musculaire.
L’inhibition systématique de l’inflammation peut retarder les processus de reconstruction myofibrillaire.
La stratégie thermique doit être réajustée en fonction de la phase lésionnelle.
La chaleur s’impose désormais comme un outil actif à intégrer dès la phase précoce de réparation post-déchirure musculaire.